研究実施
研究実施管理
臨床研究の支援として以下の業務体制を整えております。
各業務の詳細については、ボタンからリンク先をご確認ください。
実施計画書作成支援
データマネージャー、統計家による支援内容としては以下の内容が含まれます。
- 研究デザイン
- 解析計画研究デザイン
- プロトコール作成支援
- 症例報告書デザイン
- 症例登録票デザイン
統計家は、適切な研究デザイン、症例数設計、統計解析方法についてのご提案を含む研究プロトコールの作成支援を実施しており、データマネージャーはそれらの解析に耐えうるデータ収集項目のデザインの支援を実施しています。
プロジェクトマネジメント(調整事務局)業務
支援業務には例えば以下のような項目があります。ご相談に応じて必要な業務を支援します。
試験開始前
- 研究組織構築から各種試験関連文書の作成
- 試験実施体制の構築(支援体制、各種委員会選定や設置記録等作成)
- 各種文書(試験実施計画書、説明同意文書、各SOP等)の作成
- 臨床研究保険加入手続き
- 予算検討管理
- 契約締結手続き(実施医療機関、薬剤配送等外注先との契約締結における、契約書案の作成や締結先との交渉等)
- (多機関共同研究の場合)他機関への連絡、情報収集など
- 試験スケジュール策定・管理
- 安全性情報取扱体制の構築(薬剤提供者との交渉、SOPの作成)
- キックオフミーティングの開催支援
- 実施医療機関の倫理委員会/CRB申請支援
試験実施中
- 臨床試験登録/変更手続き(jRCT等)
- 薬剤配送手続き、管理
- 登録進捗管理(登録一覧表の作成、配信、登録推進業務)
- 実施医療機関等からの問合せ対応(問合せ窓口、FAQ作成)
- 安全性情報対応(医療機関、薬剤提供者、規制当局等への規定に則った報告支援)
- 監査対応(施設決定、実施医療機関と監査担当者との調整、監査報告に対する対応検討等)
- 各委員会開催支援(効安、中央判定委員会等。会議資料、議事録の作成と報告先への報告)
- 各種文書(試験実施計画書、説明同意文書雛形、各SOP等)の改訂
- 問題症例の取扱い、症例データの取扱いに関する実施医療機関間の調整
- 試験中に生じた試験実施計画書等の解釈上の疑義の調整
- 開発業務受託機関(CRO)等への業務委託(モニタリング、監査、データマネジメント、統計解析、臨床検査、その他の業務)に係る調整
- 研究費取り扱い(公的研究費の継続申請、年次報告書作成、支出管理等)
試験終了時
- 試験の中止/終了に係る調整、対応
- 薬剤回収/廃棄
- 症例検討会の開催支援(会議資料、議事録の作成と報告先への報告)
- 薬剤提供者への報告
臨床試験のニュースレター発行

サーバーにてファイル管理と情報共有

臨床試験の実施医療機関準備支援
(REDCap活用)
よくある質問(FAQ)の公開
(REDCap活用)
CRC業務
臨床研究コーディネーター(CRC)による支援の必要性
- 診療をしながら臨床研究の内容を十分把握し、必要な情報を適切な時期に確実に収集することは簡単なものではありません。
- 研究者に支援についての調査を実施したところ、「患者スケジュール管理」、「症例報告書記入、クエリー対応」の支援を求める声が最も多くありました。
今後、規制が厳しくなっていく中、計画書に記載されている規制を遵守するためにも、コーディネーターによる支援は不可欠です。 - また、倫理委員会への申請(申請システム利用)の支援を求めるお声も最近よくお聞きしています。ご要望に応じて対応を行いますのでご相談ください。
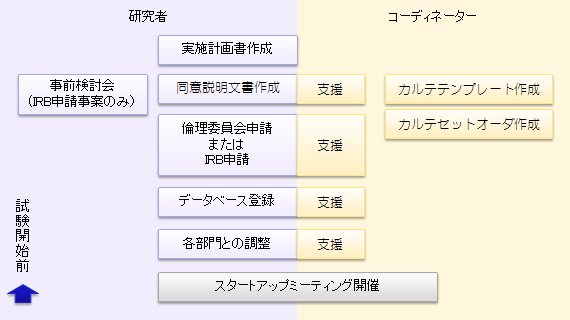
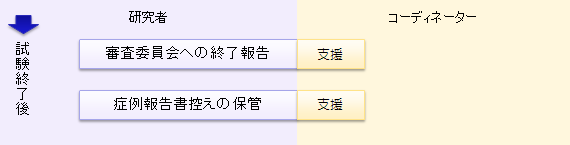
CRC業務の支援フロー
- 支援業務には下図のような項目があります。このうちご相談に応必要な部分を支援します。 例えば、症例報告書記入のみ、同意説明補助のみの支援も可能です。
健常人対象臨床研究の一斉実施
当センターでは、健常人を対象とする試験の実施を支援しています。これまでに実施した健常人対象の試験には食品介入試験、機器の介入試験、患者と健常人を対象とするコホート研究などがあります。
実施内容によって適切な実施場所を検討し、研究者にご提案します。これまで、附属病院の外来や病棟、その他にも、会議室やあべのメディックスビルなどでの実施も行ったことがあります、一斉実施の場合は、通常は週末(土日)や祝日等に実施することが多いです。
モニタリング
研究の品質確保の一環として、オンサイトまたはオフサイトモニタリングを支援いたします。
当センターで中央モニタリングもご支援させていただく場合には、オンサイトまたはオフサイトモニタリングにて、中央モニタリングのフォローアップを行い、エラーの早期修正を図ります。
また、研究者自らがモニタリング従事者として実施される場合には、必要に応じて、手順書作成支援やモニタリング報告書作成支援ツールの提供なども含め、モニタリング計画の相談をお受けしています。
オンサイト/オフサイト支援業務には以下のような項目があります。このうち研究内容に応じて必要な部分を支援します。
試験開始前
- 実施医療機関の選定の妥当性
- 手続きの妥当性
- 特定臨床研究該当性
- 実施体制の確認
- 研究計画書、同意説明分文書の適切な作成
- 必要文書の適切な保存
試験実施中
- 手続きモニタリング(変更手続き、定期報告、重篤な疾病等報告、不適合報告、薬剤等管理、必要文書の適切な保存など)
- 症例モニタリング(同意取得、適格性確認、主な実施手順とデータの確認、有害事象、不適合など)
試験終了時
- 手続き(変更手続き、定期報告、重篤な疾病等報告、不適合報告、終了報告など)
- 薬剤等管理
- 必要文書の適切な保存
監査
ただいま準備中です
薬剤管理業務
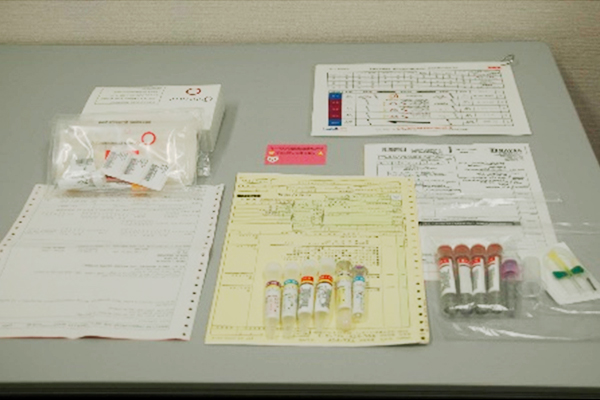
臨床試験用薬剤(白箱)の管理
保管場所が確保できない、ということはしばしば発生します。当センターが本業務を支援する場合は、治験薬管理室内で適切に管理をいたします。
ICH-GCP対応などで、温度管理、危機管理などの記録が求められる場合にも対応いたします。

お役立ちコンテンツ
●研究支援のお役立ちコンテンツはコチラから